除了血糖問題以外,近年來有非常明顯年輕化趨勢的慢性病非高血壓莫屬了。 許多3-40歲的年輕朋友們往往都是因為公司體檢,或是頭痛或是脖子緊來就診,經量測才發現竟然有血壓過高的問題。 長期未治療的高血壓會增加心血管疾病、腦中風、慢性腎病的風險。 而造成越來高血壓越普遍與年輕化的元凶,除了高壓環境、快速步調、不正常的生活作息與西化飲食外,,最重要的因素非肥胖莫屬了。 肥胖患者體內發炎物質與激素上升,交感神經系統與腎素-血管收縮素系統(RAAS)被過度活化,造成血壓升高。 據統計,體重過重的成人罹患高血壓的相對風險為BMI正常族群的2倍,輕度肥胖族群為4.2倍,而中重度肥胖族群的風險則激增為近11倍。
什麼是高血壓
血壓是當心臟收縮 ,將血液灌灌入動脈時所加諸動脈血管壁的壓力。 人體須維持正常的血 壓,才能推動血液在體內運行,將氧氣與營養物質輸送到身體各組織,供給正常運行所需。 然而,當血壓持續處於高水平,便會造成所謂的"高血壓",引發各種慢性問題。 血壓數值以兩組數字表達: 上方的收縮壓顯示心臟收縮打出血液時血管內的壓力; 下方的舒張壓則表示心臟放鬆時,動脈彈性回縮後產生流動所形成的壓力。 血壓數值會受各種不同因素影響,如身體姿勢變化、體能活動、情緒壓力、睡眠等 。
正常來說,成年人的正常血壓應<120/80 mmHg。 一般來說, 高血壓的定義是在平靜的狀態下測量血壓,連續2週內有3次以上 的血壓收縮壓≧140 mmHg,舒張壓≧90 mmHg。 本身患有冠狀動脈疾病、糖尿病、慢性腎臟疾病及使用抗血栓藥物預防中風的病人,高血壓的標準則降為≧130/80mmHg。 而在2017年AHA/ACC高血壓治療指引則將成年人的高血壓標準下修,訂定收縮壓130 mmHg以上或是舒張壓80 mmHg以上為第一期高血壓。
2017年AHA/ACC高血壓治療指引:
1. 正常血壓:收縮壓<120mmHg 且舒張壓<80mmHg。
2. 高血壓前期:收縮壓 120~129mmHg且舒張壓<80mmHg。
3. 高血壓第1期:收縮壓 130~139 mmHg 或舒張壓 80~89 mmHg。
高血壓第2期:收縮壓 ≧140 mmHg或舒張壓≧90 mmHg。
就兒童或青少年而言,如果重複量度的收縮壓或舒張壓數值等於或高於同年齡 、高度和性別 平均血壓的第95 百分位數,則表示患有高血壓 。
肥胖是如何造成高血壓的?
早在1980年代,研究就發現"上半身"肥胖的患者較下班身肥胖的人更容易罹患心血管疾病與代謝症候群。 上半身肥胖可進一步用"腰臀圍比率"量化,當此比率越高,得到高血壓、心肌梗塞、血脂異常與第二型糖尿病的機會也越大。 當人體攝入過高熱量時,這些多餘的熱量負荷與高脂高碳水成分會造成周邊正腎上腺素周轉傳遞(peripheral noradrenaline turnover)增加,刺激α1 and β-腎上腺周邊接收器,使交感神經系統活性上升。 此外,血中高濃度的發炎性細胞激素也會影響血管內皮功能,游離性脂肪酸同時也會增加α-腎上腺素血管敏感性,進而提高動脈張力。 研究顯示,中心脂肪(內臟脂肪)越高,交感神經系統活性也隨之提高。此外,脂肪細胞還會影響腎素-血管收縮素系統,使血壓上升,同時影響腎功能。 我們接下來將針對上述途徑做進一步的探討。
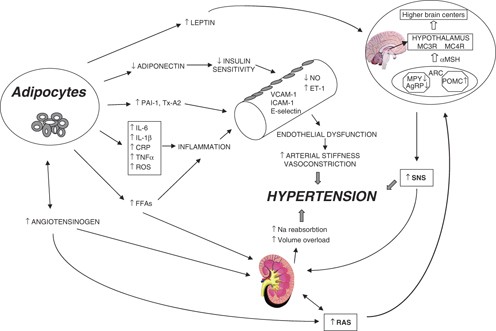
脂肪組織影響內分泌
許多人不知道,脂肪細胞其實在我們的內分泌系統扮演了重要的角色。 除了發炎性細胞激素以外,脂肪細胞會分泌許多特殊的脂肪細胞素,如瘦素(leptin)、阻抗素(resistin),以及抗發炎物質如脂聯素 (adiponectin)、乙型轉化生長因子(TGF-beta)、介白質-10(IL-10)、一氧化氮(NO)等。 瘦素作用於我們腦部下視丘的瘦素受體,可活化 POMC 路徑,進而抑制食慾並增加能量消耗,以及抑制腦部刺激食慾之NP-Y分泌。 瘦素對週邊組織,如肌肉和肝臟,有調節胰島素敏感性的作用。 當脂肪組織增加,分泌出的瘦素也等比例上升。 瘦素會通過血腦屏障,在抑制食慾的同時增加能量消耗與交感神經活性以及抑制一氧化氮生產。 低濃度的一氧化氮會使血管內皮緊縮與功能失調,使張力增加,造成血壓升高。
脂聯素主要由脂肪組織所製造分泌之蛋白質,具有調節能量代謝、改善胰島素阻抗及減緩動脈粥狀硬化的作用。 脂聯素作用於單磷酸腺苷活化蛋白質激酶(5’AMP-activated protein kinase),可以抑制脂肪酸生成、減低醣質新生並且增加肌肉對血糖的吸收來降低血糖。 研究顯示,BMI正常的族群體內脂聯素濃度較高,而患有第二型糖尿病與冠心症的肥胖患者體內濃度則有明顯的低下。 研究指出,較低的脂聯素濃度會使周邊組織的胰島素敏感性下降,造成胰島素阻抗。 進而抑制血管內皮細胞上黏著分子的表現,降低一氧化氮分泌,造成血管內皮功能失調,動脈硬化與血管緊縮等問題。 另一方面,胰島素阻抗迫使更多胰島素被分泌出。 高胰島素濃度便會直接作用於腎臟,使鈉離子回收與水分滯留增加。 當整體水分過多,血壓便會上升。
最後,由脂肪組織釋放出的內生性大麻神經傳導物質(endocannabinoids)如花生四烯乙醇(anandamide)與2-花生四烯酸甘油酯(2-arachidonoylglycerol)會影響食慾以及葡萄糖與脂肪代謝。 肥胖患者體內因胰島素阻抗與發炎物質濃度上升,刺激內生性大麻神經傳導物質的過度表現,進而造成內臟脂肪過度堆積與脂聯素濃度下降。 近年的最新研究發現,過高的內生性大麻神經傳導物質與肥胖相關的併發症如腎病變、動脈粥狀硬化和心臟疾病有密切相關。
肥胖影響腎素-血管收縮素系統造成腎病變
肥胖患者體內的腎素、血管收縮素、醛固酮濃度上升,影響腎素-血管收縮素系統平衡。 交感神經系統經由各種途徑被活化後,刺激腎素與血管收縮素II的分泌。 此外,肥胖細胞(特別是內臟脂肪組織)也會生產製造血管收縮素元,促進血管收縮素II與醛固酮的分泌。 這些分子會增加腎素-血管收縮素系統的活性,造成血管緊縮與體液容量過高,使血壓上升。 另一方面,由於肥胖患者腎髓質周圍脂肪組織過多造成壓迫,使腎素分泌不會因為體液容量上升而被抑制,使腎素-血管收縮素系統持續的活化,造成長期的高血壓。 慢性的高血壓問題會使腎絲球過濾長期上升,使腎小管肥大硬化,最終導致腎小管壞死,引起後續諸多的併發症,如心血管疾病、腎病變,甚至是末期腎臟疾病。
肥胖與高血壓共同增加心血管疾病風險
高血壓是多種心血管疾病,含冠心症、中風、心臟衰竭、主動脈與周邊動脈及瓣膜性心臟病的重要高風險因子。 研究指出,肥胖會加重高血壓併發上述心血管疾病的風險。 美國芝加哥心臟學會發表於"心臟學"期刊的論文發現,BMI越高的患者,高血壓併發心血管疾病的死亡率越高,且與BMI呈線性正相關。 此外,冠心症和中風的住院率與死亡率也更高。 另一方面,除了高血壓以外,肥胖導致的胰島素阻抗也顯著的提高第二型糖尿病的罹病率。而血糖問題本身就是導致心血管疾病的高風險因子。 當此三項加總再一起,對健康產生的威脅自然不容小覷。
積極控制血壓可有效降低心血管風險
2015年發表於新英格蘭期刊的大型研究SPRINT發現,嚴格控制血壓(收縮壓<120 mmHg)可有效降低心血管事件以及死亡率。 而追蹤原受試者3.88年的結果更指出,試驗終止後即使病人後續不再特別嚴格控制血壓,心血管疾病發生率及死亡率仍然較低。 2021年牛津大學發表於Lancet的多國床試驗統合分析研究發現,每降5 mmHg的收縮壓,可減少9~11%的心血管事件,且此結果不因年齡高低而有所改變。 在台灣,台大醫院的研究顯示,患有高血壓的60~80歲長者,嚴格控制血壓至110~130mmHg的患者相對於130~150mmHg的族群,心血管風險下降了26%。 由此可知,積極控制血壓可有效降低心血管疾病風險。
對於合併肥胖與高血壓的患者來說,除了藥物治療以外,減重可有效改善血壓問題。 在減重初期,應搭配血壓藥物將血壓控制至正常數值,同時也降低併發左心肥大與第二型糖尿病的比率,減少幅度可達三成。 此外,由於肥胖患者若合併睡眠呼吸中止問題,對血壓控制帶來不良影響,也應在減重期間接受治療。 目前市面上已有安全合法之減重藥物,搭配生活習慣調整與運動,都可協助患者達到有效減重減脂,改善高血壓等慢性問題。
資料來源:
1. Leggio, M., Lombardi, M., Caldarone, E. et al. The relationship between obesity and hypertension: an updated comprehensive overview on vicious twins. Hypertens Res 40, 947–963 (2017). https://doi.org/10.1038/hr.2017.75
2. Obesity and hypertension
Shu-Zhong Jiang, Wen Lu, Xue-Feng Zong, Hong-Yun Ruan, Yi Liu
Exp Ther Med. 2016 Oct; 12(4): 2395–2399. Published online 2016 Sep 6. doi: 10.3892/etm.2016.3667